Faudra aussi faire l'historique de tout ça et en plus en plusieurs langues. Il y a des livres comme celui de D. van Monckhoven de 1884 plein de formules anciens dans des termes obsolètes. Et encores des livres de Agfa en Néerlandais des années 60-70 plein de formules. Ou des livers en allemands des années '30. On peut trouver tout ça soit en .pdf sur le net, soit dans des magazins de récyclage. Et il reste alors encore les mésures anciens...
C'est toute une spécialité je pense. Mais je vais suivre tout ce qui passe ici.
Chimie et photo : vos questions
-
Havoc
- Super Gourou

- Messages : 6946
- Enregistré le : jeudi 31 mars 2011 19:07
- Localisation : Galactic Sector ZZ9 Plural Z Alpha
- Oriu
- Membre de l'association

- Messages : 36587
- Enregistré le : lundi 21 avril 2008 18:37
- Localisation : 37 mais 2A par le coeur
Re: Chimie et photo : vos questions
Pour l'hypoclear et d'autres produits destinés à faciliter l'élimination des résidus d'hyposulfite de Sodium ou autres résidus du fixateur, l'ajout d'une pincée de Sulfite ou de bicarbonate de soude des écolos du ménage, permet d'augmenter l'élimination.
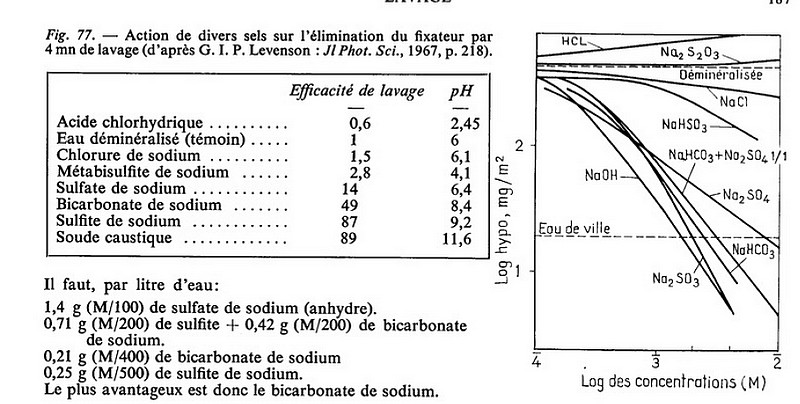
je remet un graphe publié dans un livre de Glafkidés, on remarque par exemple qu'un peu de bicarbonate (NaHCO3) augmente l'efficacité du lavage.
Comptez pas sur moi pour une explication du graphe ni des mécanismes d'échange chimique, il manque dans le tableau efficacité de lavage de l'eau de ville par rapport à l'eau déminéralisée, je sais, ça dépend de quelle eau de ville, selon qu'on habite en région granitique ou calcaire l'efficacité du lavage est très variable.
je remet un graphe publié dans un livre de Glafkidés, on remarque par exemple qu'un peu de bicarbonate (NaHCO3) augmente l'efficacité du lavage.
Comptez pas sur moi pour une explication du graphe ni des mécanismes d'échange chimique, il manque dans le tableau efficacité de lavage de l'eau de ville par rapport à l'eau déminéralisée, je sais, ça dépend de quelle eau de ville, selon qu'on habite en région granitique ou calcaire l'efficacité du lavage est très variable.

-
Havoc
- Super Gourou

- Messages : 6946
- Enregistré le : jeudi 31 mars 2011 19:07
- Localisation : Galactic Sector ZZ9 Plural Z Alpha
Re: Chimie et photo : vos questions
Oui, ce grafique est un peu difficile à lire. En verticale il y a le log (base 10) du concentration de hypo qui reste après un lavage de 4 minute dans la solution. En horizontale par contre c'est la valeur absolue du log (base 10) de la concentration en molaire utilisé au début de lavage. Chaque courbe représente donc la concentration finale de hypo à la fin d'un lavage de 4 minutes si on commence avec la concentration en bas du grafique.Oriu a écrit : mercredi 25 février 2026 7:04 Pour l'hypoclear et d'autres produits destinés à faciliter l'élimination des résidus d'hyposulfite de Sodium ou autres résidus du fixateur, l'ajout d'une pincée de Sulfite ou de bicarbonate de soude des écolos du ménage, permet d'augmenter l'élimination.
je remet un graphe publié dans un livre de Glafkidés, on remarque par exemple qu'un peu de bicarbonate (NaHCO3) augmente l'efficacité du lavage.
Comptez pas sur moi pour une explication du graphe ni des mécanismes d'échange chimique, il manque dans le tableau efficacité de lavage de l'eau de ville par rapport à l'eau déminéralisée, je sais, ça dépend de quelle eau de ville, selon qu'on habite en région granitique ou calcaire l'efficacité du lavage est très variable.

Comme 0.21 g de NaHCO3 dans 1 litre d'eau (pure) est 1/400-ième de molaire, il faut regarder a 2.6 sur l'axe horizontale et puis monter jusqu'à la courbe de NaHCO3. Donc environs aussi efficace que l'eau de robinet.
Comme la distance entre la ligne de l'eau déminéralisé et celle de l'eau de robinet est environ la même que entre 1 et 2 de l'axe verticale, l'eau de robinet est environs à "10" comme efficacité.
- Oriu
- Membre de l'association

- Messages : 36587
- Enregistré le : lundi 21 avril 2008 18:37
- Localisation : 37 mais 2A par le coeur
Re: Chimie et photo : vos questions
On voit que c'est le mélange Bicarbonate de Sodium + Sulfate de sodium qui permet de descendre le plus bas après 4mn
le Sulfate de Sodium n'est pas cher 6,1 euros le kg https://www.mon-droguiste.com/sulfate-d ... hydre.html
ajouté au bicarbonate ça fait du washaid à pas cher !
le Sulfate de Sodium n'est pas cher 6,1 euros le kg https://www.mon-droguiste.com/sulfate-d ... hydre.html
ajouté au bicarbonate ça fait du washaid à pas cher !
-
Havoc
- Super Gourou

- Messages : 6946
- Enregistré le : jeudi 31 mars 2011 19:07
- Localisation : Galactic Sector ZZ9 Plural Z Alpha
Re: Chimie et photo : vos questions
1 kg de NaSO4 fait alors 1.4 m³ de washaid....
- numérix
- Super Gourou

- Messages : 8800
- Enregistré le : lundi 10 avril 2006 20:37
- Localisation : pas loin de Tours
- Contact :
Re: Chimie et photo : vos questions
et ça évite d'avoir la gélatine dans les chaussettesOriu a écrit : mercredi 25 février 2026 9:41 On voit que c'est le mélange Bicarbonate de Sodium + Sulfate de sodium qui permet de descendre le plus bas après 4mn
le Sulfate de Sodium n'est pas cher 6,1 euros le kg https://www.mon-droguiste.com/sulfate-d ... hydre.html
ajouté au bicarbonate ça fait du washaid à pas cher !



